|
Secretaris-Generaal VN
Geregistreerd: 18 mei 2005
Locatie: Limburg
Berichten: 50.229
|
 Grote stap tegen kanker?
Grote stap tegen kanker?
Citaat:
https://www.vrt.be/vrtnws/nl/2018/02...uitzaaiing--e/
Luc De Roy
vr 02 feb 20:31
Injectie schakelt kankers uit bij muizen, zelfs na uitzaaiïng, en wordt weldra getest bij mensen
Een inspuiting tegen kanker die bij muizen tumoren kan uitschakelen, zelfs als ze uitgezaaid zijn in het lichaam, wordt weldra getest bij een kleine groep mensen. Onderzoekers van de Stanford University in Calfornië hebben ontdekt dat het rechtstreeks in een tumor inspuiten van minieme hoeveelheden van twee middelen die het immuunsysteem activeren, niet alleen die tumor doodt, maar ook een "verbazingwekkende reactie in heel het lichaam" uitlokt die niet behandelde verafgelegen uitzaaiïngen vernietigt.
Uit de nieuwe studie blijkt dat de behandeling toegepast kan worden op veel verschillende soorten kankers. De onderzoekers denken dat de plaatselijke toediening van zeer kleine hoeveelheden van de stoffen kan dienen als een snelle en relatief goedkope therapie tegen kanker, en dat het onwaarschijnlijk is dat de behandeling de kwalijke neveneffecten zal veroorzaken die vaak gezien worden bij een stimulatie van het immuunsysteem in heel het lichaam.
"Als we die twee stoffen samen gebruiken, zien we dat tumoren in heel het lichaam uitgeschakeld worden", zei Ronald Levy op de website van Stanford. Levy is professor oncologie, en een van de hoofdauteurs van de studie. "Deze aanpak vermijdt de noodzaak om tumor-specifieke doelwitten voor het immuunsysteem te identificeren, ze vereist geen algehele activering van het immuunsysteem, en evenmin een aanpassing van de immuuncellen van de patiënt."
"Verbazende effecten doorheen heel het lichaam"
Professor Levy is een pionier op het vlak van kanker-immunotherapie, waarbij onderzoekers trachten het immuunsysteem in te schakelen in de strijd tegen kanker. Onderzoek in zijn laboratorium heeft geleid tot de ontwikkeling van rituximab, een van de eerste monoklonale antilichamen die goedgekeurd zijn als middel tegen bepaalde kankers bij mensen.
Sommige benaderingen op het gebied van immunotherapie zijn gebaseerd op het stimuleren van het immuunsysteem doorheen heel het lichaam, andere therapieën richten zich natuurlijk voorkomende "controleposten" die de anti-kanker-activiteit van immuuncellen beperken. Bij nog andere, zoals de CAR T-cel-therapie die onlangs goedgekeurd is voor de behandeling van sommige soorten leukemie en lymfomen -bloed- en lymfe(klier)kankers -, moeten de immuuncellen van een patiënt uit het lichaam worden gehaald en genetisch behandeld worden om de tumoren aan te vallen. Veel van die benaderingen zijn succesvol gebleken, maar ze hebben ook nadelen, van moeilijk te behandelen neveneffecten tot hoge kosten en lange voorbereidings- of behandelingstijden.
"Al deze doorbraken op het vlak van immunotherapie veranderen volop de medische praktijk", zo zei Levy. "Onze aanpak gebruikt een eenmalige toediening van zeer kleine hoeveelheden van twee actieve stoffen die de immuuncellen enkel in de tumor zelf stimuleren. Bij de muizen zagen we verbazingwekkende effecten doorheen heel het lichaam, waaronder de uitschakeling van tumoren overal in het dier."
Kankers leven vaak in een raar soort van tweestrijd met het immuunsysteem. Immuuncellen zoals de T-cellen herkennen de abnormale proteïnen die vaak aanwezig zijn op kankercellen, en infiltreren dan de tumor om hem aan te vallen. Als de tumor groeit, "bedenkt" hij echter vaak manieren om de activiteit van de T-cellen te onderdrukken.
De methode van Levy en zijn team werkt door de kanker-specifieke T-cellen te reactiveren door rechtstreeks in de tumor enkele microgrammen - een miljoenste van een gram - te injecteren van twee actieve stoffen. De ene stof, een kort stukje DNA dat een CpG oligonucleotide genoemd wordt, werkt samen met andere immuuncellen in de buurt om de expressie - de werking - te versterken van de activeringsontvanger OX40 op het oppervlak van de T-cellen. De andere stof, een antilichaam dat zich bindt aan OX40, activeert de T-cellen om ten strijde te trekken tegen de kankercellen. Omdat de twee stoffen rechtstreeks in de tumor geïnjecteerd worden, worden alleen de T-cellen geactiveerd die de tumor al geïnfiltreerd hebben. In feite zijn die T-cellen "voorgescreend" door het lichaam om enkel kanker-specifieke proteïnen te herkennen.
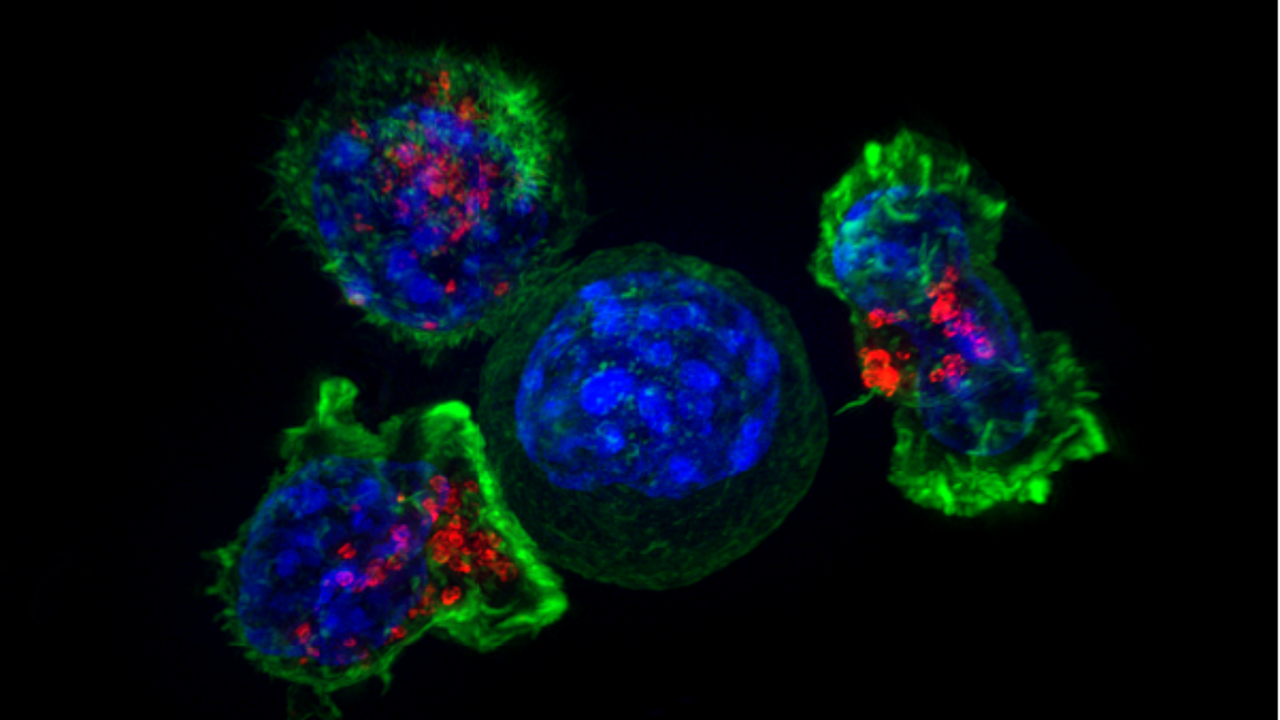
Superresolutie beeld van een groep killer T-cellen (blauw met groen en rood) die een kankercel (blauw, midden) omcirkelen. Als een killer T-cel contact maakt met een doelwitcel, maakt de killercel zich vast aan het gevaarlijke doelwit, en spreidt ze zich er over uit. De killercel gebruikt dan speciale chemische stoffen die bewaard worden in vesikels, afgesloten blaasjes (rood), om de kankercel te doden. Die gebeurtenis wordt daarom ook de "kus des doods" genoemd. Als de doelwitcel gedood is, gaat de killer T-cel op zoek naar een volgend slachtoffer. (foto: US National Institutes of Health)
Kanker-vernietigende zwervers
Een aantal van deze tumor-specifieke, geactiveerde T-cellen, verlaten dan de originele tumor om op zoek te gaan naar identieke tumoren doorheen heel het lichaam, en die te vernietigen.
De aanpak werkte verrassend goed met laboratoriummuizen bij wie tumoren van muizenlymfoom getransplanteerd waren op twee plaatsen in hun lichaam. Het injecteren van één tumor met de twee middelen, veroorzaakte niet enkel de regressie van de behandelde tumor, maar ook van de tweede, niet behandelde tumor. Op die manier werden 87 van de 90 muizen genezen van kanker. Bij drie van de muizen kwam de kanker terug, maar die verdween opnieuw na een tweede behandeling. De onderzoekers zagen gelijkaardige resultaten bij muizen met borstkanker-, karteldarmkanker- en melanoomtumoren.
Muizen die genetisch aangepast waren om spontaan borstkanker te krijgen aan alle tien hun tepels, reageerden eveneens gunstig op de behandeling. Het behandelen van de eerste tumor die verscheen, verhinderde vaak het opduiken van latere tumoren, en verlengde aanzienlijk de levensduur van de dieren, zo ontdekten de onderzoekers.
Citaat:
Ik denk niet dat er een grens is aan het soort van tumoren dat we potentieel zouden kunnen behandelen, zo lang ze maar geïnfiltreerd zijn door het immuunsysteem.
Professor Ronald Levy
|
Ten laatste onderzocht mede-hoofdauteur Idit Sagiv-Barfi de specificiteit van de T-cellen door twee soorten van tumoren in de muizen te transplanteren. Ze transplanteerde dezelfde lymfoom-kankercellen in twee plaatsen, en een karteldarmkanker in een derde plaats. De behandeling van een van de lymfoomtumoren veroorzaakte de regressie van de beide lymfoomtumoren, maar had geen effect op de groei van de karteldarmkankercellen.
"Dit is een zeer gerichte benadering", zei Levy. "Enkel de tumor die dezelfde proteïnedoelwitten heeft als de behandelde tumor, wordt getroffen. We vallen specifieke doelen aan zonder dat we precies moeten identificeren welke proteïnen de T-cellen herkennen."
De onderzoekers zijn een klinische proef begonnen, waarvan verwacht wordt dat er 15 patiënten met niet al te agressief lymfoom voor gerecruteerd zullen worden. Als die succesvol zijn, gelooft Levy dat de behandeling nuttig zou kunnen zijn voor vele soorten van tumoren. Hij ziet een toekomst waarin klinische medici de twee stoffen injecteren in vaste tumoren bij mensen, voorafgaand aan de chirurgische verwijdering van de kanker. Op die manier zou men het terugkeren van de tumoren door niet geïdentificeerde uitzaaiïngen kunnen verhinderen, of zelfs de ontwikkeling van toekomstige tumoren die voort zouden komen uit genetische mutaties zoals BRCA1 en 2, kunnen voorkomen.
"Ik denk niet dat er een grens is aan het soort van tumoren dat we potentieel zouden kunnen behandelen, zo lang ze maar geïnfiltreerd zijn door het immuunsysteem", zo zei Levy.
De studie van het team van Stanford is gepubliceerd in "Science Translational Medecine".
Citaat:
http://stm.sciencemag.org/content/10/426/eaan4488
Eradication of spontaneous malignancy by local immunotherapy
Idit Sagiv-Barfi1, Debra K. Czerwinski1, Shoshana Levy1, Israt S. Alam2, Aaron T. Mayer2, Sanjiv S. Gambhir2 and Ronald Levy1,*
See all authors and affiliations
Science Translational Medicine 31 Jan 2018
|
|
Laatst gewijzigd door Micele : 3 februari 2018 om 14:27.
|